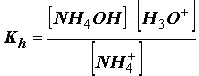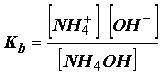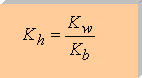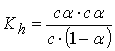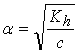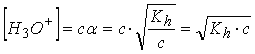|
En este caso, el anión no se hidrolizará ya que proviene de un ácido fuerte, pero si se hidrolizará el catión ya que proviene de una base débil. Darán lugar a soluciones acuosas ácidas puesto que el catión reacciona con el agua para dar protones. Vamos a ver un ejemplo con la sal de cloruro amónico (NH4Cl):
el anión no reaccionará con el agua al provenir de un ácido fuerte:
Cl-
+ H2O el catión al provenir de una base débil reacciona con el agua de la siguiente manera (y ésta es la reacción de hidrólisis):
NH4+
+ 2 H2O la constante de esta reacción de hidrólisis será:
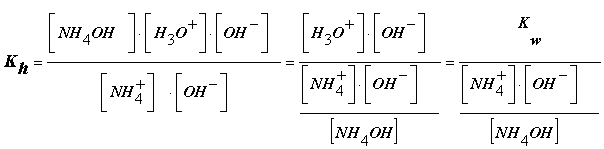
si multiplicamos y dividimos por [OH-] resulta:
por otra parte:
luego:
esta ecuación nos permite calcular la constante de hidrólisis conociendo Kw y la constante de disociación de la base débil (Kb). Es fácil calcular la concentración de protones si se conoce la concentración de la sal en disolución (c) y la fracción de dicha sal que se hidroliza (a). Vamos a verlo con un ejemplo:
ya que la reacción está totalmente desplazada. Como el catión proviene de una base débil se hidrolizará según la siguiente ecuación química:
sustituyendo en la constante de hidrólisis resulta:
si Kh < 1O-4, entonces a se puede despreciar frente a 1 y resulta que:
de donde:
y una vez determinado la concentración de protones, ya podemos calcular el pH que dejará la disolución de dicha sal (y el pOH). pH = ‑ log [H3O+] pOH = 14 - pH recordemos que en la hidrólisis de sales de ácido fuerte – base débil, la disolución resultante debe ser ácida, por lo que el pH calculado debe ser inferior a 7.
|